Von Hippel definió el Glaucoma Pigmentario (GP) como la asociación de un Síndrome de Dispersión Pigmentaria (SDP) e Hipertensión Ocular (HTO). Para algunos autores esta definición sigue siendo válida, mientras que otros prefieren referirse a GP una vez que se han producido cambios evidenciables en el estudio estructural del nervio óptico o aparecen defectos típicos en el campo visual. De cualquier manera, se trata de una disquisición semántica, puesto que, la mayor parte de las veces, el SDP es la consecuencia de una anomalía anatómica, que la mayoría de las veces, en un tiempo variable, y si no se trata, termina desembocando en un cuadro inequívocamente glaucomatoso.
Se trata de una enfermedad típica de la raza caucásica, aunque recientemente hay autores que defienden que en la raza negra permanece infradiagnosticada, por la mayor pigmentación fisiológica típica de esta etnia, que tiende a enmascarar los cambios típicos de este síndrome. Suele tratarse de pacientes con miopías bajas a moderadas (0 a -5 dioptrías), y por sexos predominan los varones. La tasa de conversión de SDP a GP corre paralela a la magnitud de la miopía, es decir, a mayor miopía, mayor riesgo de glaucoma pigmentario, en presencia de SDP.

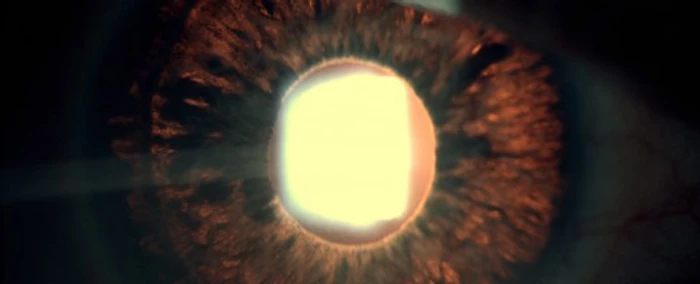
Dicha alteración anatómica, se caracteriza por una forma especial de insertarse el iris en el cuerpo ciliar. Algunos autores hacen referencia a que “da la sensación de que el iris es demasiado grande, y necesita plegarse”. En la lámpara de hendidura llama la atención una desmesurada profundidad de la cámara anterior. Gonioscópicamente el rasgo más representativo es la concavidad de la periferia del iris, mientras que el resto se halla desplazado posteriormente, en íntimo contacto con el cristalino, y extremadamente cerca de la zónula (a veces, hay fibras zonulares muy anteriores, que se insertan muy centralmente en la cápsula anterior del cristalino). En estas condiciones, es fácil entender que los movimientos intrínsecos (acomodación), extrínsecos (rotación ocular alrededor de sus ejes), parpadeo, frotamiento ocular, maniobras de Valsalva, y en general todo lo que altere la posición de las estructuras oculares o los cambios transitorios de presión intraocular, incremente el rozamiento entre la capa pigmentaria posterior del iris con el cristalino y la zónula, liberándose pigmento, células y otros elementos, en cantidad variable. Se produce además un fenómeno curioso, y es que, debido a la posición del iris, la presión en la cámara anterior es ligeramente mayor que en la posterior, dando lugar a lo que se ha denominado “bloqueo pupilar inverso” que se manifiesta más intensamente cuando por la acomodación, el cristalino es empujado hacia adelante.

Foto derecha: gonioscopía del cuadrante inferior del ángulo del mismo paciente. Igualmente lleno de pigmento
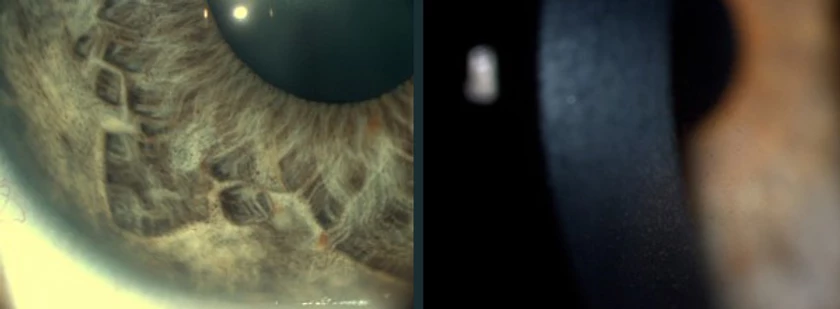
Foto derecha: pigmento en endotelio corneal (Huso de Krukenberg)
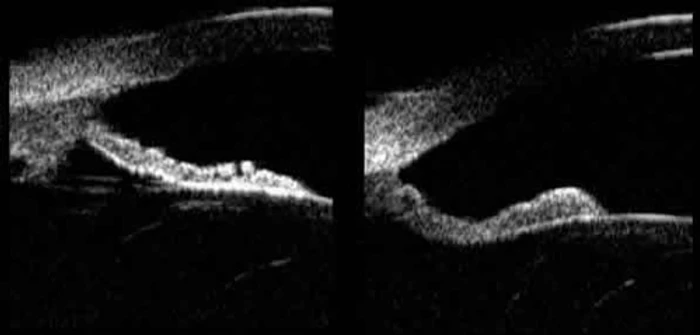
Esta dinámica alterada del iris ha sido estudiada exhaustivamente mediante biomicroscopía ultrasónica (BMU) por el Prof. García Feijoo y Cols. Unido a esta configuración anatómica, parece haber anomalías intrínsecas del iris que determinan una mayor facilidad para la pérdida de pigmento, que tienen una base genética. La movilización masiva de pigmento por el ejercicio físico intenso puede determinar elevaciones tensionales muy acusadas. La instilación de pilocarpina al 2% puede prevenir este fenómeno.
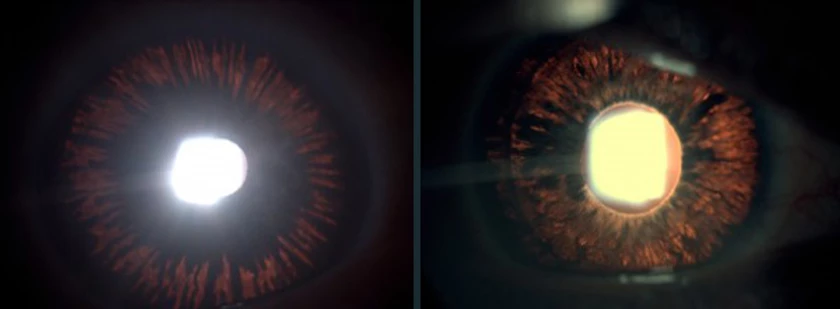
Foto derecha: transiluminación del iris en un caso grave de SDP. Patrón difuso
Pero si el pigmento cambia de sitio, lógicamente, desaparece de su lugar habitual. Por esta razón, cuando la movilización pigmentaria alcanza una intensidad importante, aparecen defectos al observar el iris por transiluminación (signo de la rueda de carro). En ocasiones, la desaparición del pigmento de la cara posterior del iris puede ser tan marcada, que el patrón sea difuso.
La historia natural de esta enfermedad tiene tres fases diferenciadas:
Fase de dispersión pigmentaria activa: Suele comenzar en la adolescencia, a lo largo de la segunda década de la vida. La inmensa mayoría de las veces es asintomática, y la PIO habitualmente es normal. Sin embargo, la dispersión pigmentaria se puede acelerar como respuesta a diversos factores ambientales, como ejercicio físico, estrés, midriasis fisiológica o inducida farmacológicamente (la fenilefrina puede ocasionar una movilización pigmentaria masiva en algunos casos). A pesar de todo ello, la PIO no tiene porqué aumentar en todos los casos en esta fase.
Fase de conversión a glaucoma: Recientemente se ha estimado que la tasa de conversión de SDP a GP es del 10% en 5 años, y aumenta al 15% a los 15 años. Otros autores han informado de una tasa del 35% en un lapso de tiempo variable entre 5 y 35 años desde el momento de inicio de la dispersión de pigmento. Como ya hemos comentado, la miopía elevada es un factor de riesgo para la conversión de SDP a GP.
Fase de (posible) regresión: Algunos pacientes con GP mejoran con la edad. El pigmento comienza a eliminarse de la malla trabecular, y ésta recupera cierto grado de funcionalidad, descendiendo la PIO hasta niveles normales. Si el diagnóstico de glaucoma se hace en esta fase, la alteración neurológica y campimétrica puede hacernos cometer el error de etiquetarlo como glaucoma normotensivo (GNT). Para distinguirlos, es útil el estudio gonioscópico, en el que llama la atención encontrar mayor densidad de depósito pigmentario en los cuadrantes superiores que en los inferiores (signo de la “inversión pigmentaria”), aunque no es específico de esta situación, ya que está presente siempre que se produce un aclaramiento espontáneo de pigmento en la malla trabecular.
El algoritmo de tratamiento del GP, al igual que otros glaucomas de ángulo abierto, se basa en un descenso de la PIO hasta niveles supuestamente seguros, considerados individualmente, en función de los resultados de los estudios estructurales y funcionales realizados a lo largo del seguimiento. Sin embargo, sus particularidades determinan ciertas especificidades que conviene reseñar.
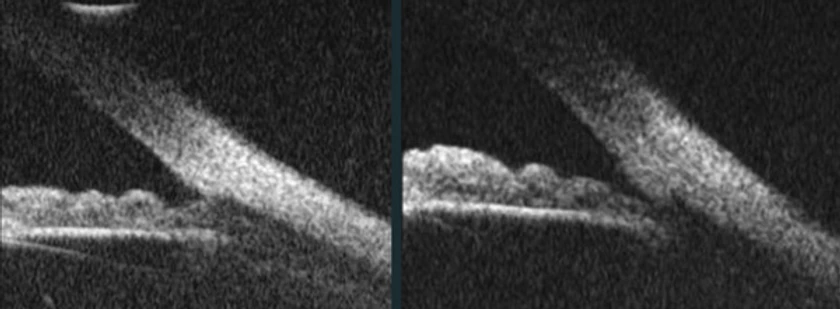
Foto derecha: GP tras la aplicación de pilocarpina al 2%. El iris ha ganado convexidad, al cerrarse la pupila y aumentar el gradiente de presión en la cámara posterior.
En cuanto al tratamiento médico, los fármacos que reducen el contacto entre la superficie posterior del iris y la zónula, como los mióticos (pilocarpina) han sido utilizados profusamente en el pasado. La pilocarpina revierte el bloqueo pupilar inverso, rectifica la posición del iris, reduce la liberación de pigmento y aumenta la facilidad de salida del humor acuoso, con lo que consigue la reducción de la PIO. Sin embargo, al tratarse de pacientes jóvenes, miopes, la pilocarpina no suele tolerarse bien, por incrementar el defecto refractivo, empeorar la visión nocturna y producir dolor. Además, si tenemos en cuenta que los pacientes con SDP /GP tienen mayor riesgo de alteraciones regmatógenas retinianas y por consiguiente de desprendimiento de retina, el tratamiento con mióticos incrementa este riesgo. Los fármacos que aumentan el flujo de salida, como las prostaglandinas son eficaces en el GP, pero lo hacen mediante el incremento del flujo de salida uveoescleral, sin que influyan en la liberación de pigmento, la dispersión y deposición de éste y el grado de obstrucción de la malla trabecular.
Trabeculoplastia láser, tanto con láser de argón (ALT) como selectiva (SLT). Ambas pueden ser una opción razonable. Al contrario de lo observado en el glaucoma primario de ángulo abierto (GPAA), la trabeculoplastia láser funciona mejor en pacientes jóvenes con GP, siendo peores los resultados, cuanto más tiempo haya transcurrido desde el inicio de la enfermedad. Desde el punto de vista técnico, deberemos tener mucho cuidado con no aplicar un exceso de energía, que desencadene picos tensionales, que son más frecuentes en este tipo de glaucoma. En la literatura se habla de potencias de 300 mw por impacto en ALT y de 0,4 mj en SLT. Sin embargo, en mi experiencia procuro guiarme por conseguir el efecto deseado en cada impacto sin preocuparme del nivel de energía (burbuja pequeña en el lugar del impacto para ALT y liberación de “burbujas de champán” en el 50% de los disparos en la SLT). Normalmente consigo estos objetivos con potencias más bajas que las descritas, aunque dependiendo del estado de cada equipo, esto puede variar. Administramos alfa-agonistas (brimonidina) solos o en combinación fija con betabloqueantes, dos veces al día durante 2 semanas, para prevenir los picos tensionales. En el caso de la SLT es especialmente importante procurar no solapar los disparos.
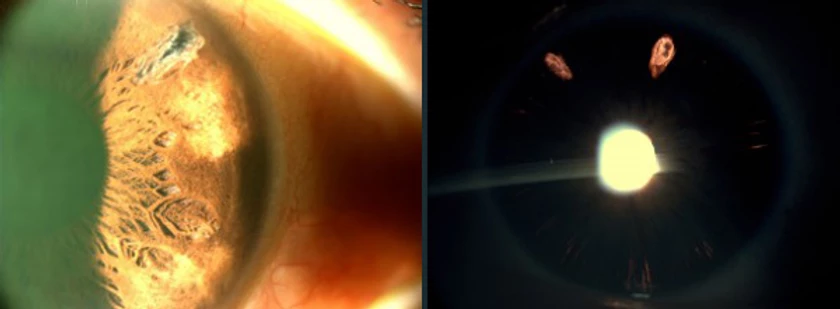
Foto derecha: doble IP. A pesar de los cambios fisiológicos de gradiente de presión entre ambas cámaras, el iris no va a cambiar su posición.
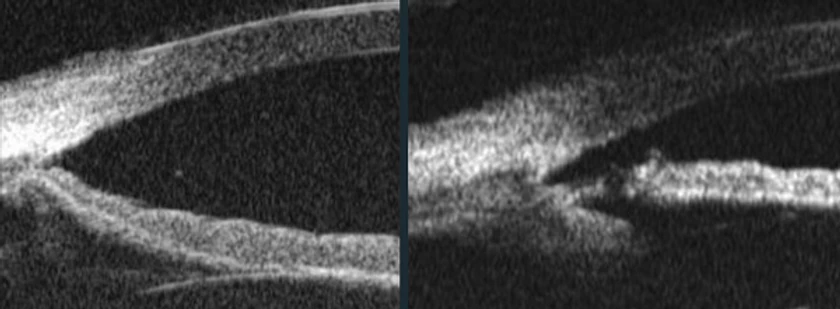
Foto derecha: SDP. Rectificación de la concavidad del iris tras la IP
Iridotomía láser. Una iridotomía periférica (IP) suficientemente amplia, o incluso doble, además de corregir la posición del iris, lo estabiliza, haciéndolo inmune a los desplazamientos acuosos producidos por los cambios fisiológicos de gradiente de presión entre las diferentes cámaras del ojo. En ojos con SDP, la iridotomía YAG disminuye en un 65% el pigmento circulante. Tiene el inconveniente de que libera abundante pigmento en el momento de su realización, por lo que los picos tensionales tras el tratamiento no son infrecuentes, lo que deberemos tener en cuenta para prevenirlos médicamente, añadiendo corticoides tópicos y acetazolamida oral a los alfa-agonistas. La IP ha demostrado reducir significativamente la conversión de SDP a GP, siendo más evidente este beneficio en pacientes por debajo de 40 años de edad. Si bien la IP ha probado su eficacia en la reducción de la liberación de pigmento, no lo es tanto para reducir la PIO, aunque no es el objetivo primordial directo de la IP en el GP. Los beneficios en cuanto a la reducción de la PIO debidos a la IP en el GP han de ser contemplados a largo plazo. En pacientes con GP de larga evolución en los que el trabeculum está muy obstruido, la utilidad de la IP es controvertida.
Sin embargo, en nuestra experiencia, hemos podido constatar cómo la rectificación de la concavidad del iris periférico mediante la realización de iridotomías periféricas consigue frenar la dispersión de pigmento, permitiendo regenerarse la capa pigmentaria del iris. En fotografías sucesivas, tomadas con varios meses de diferencia, antes y después de las iridotomías, puede observarse claramente cómo la cantidad de pigmento en esta capa del iris aumenta, coincidiendo con un mejor control tensional, en una paciente a la que, por otra parte se le ha sometido a tratamiento con SLT. La acción conjunta de la trabeculoplastia y la detención de la dispersión de pigmento, ha permitido una reducción de su medicación, obteniéndose a la vez cifras de PIO más bajas. Las fotografías hablan por sí mismas.
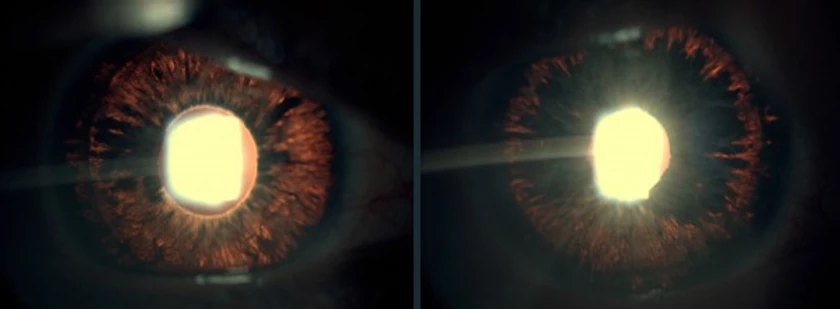
Foto derecha: el ojo izquierdo de la misma paciente. Aunque importante, la pérdida de pigmento es menor que en el ojo contralateral
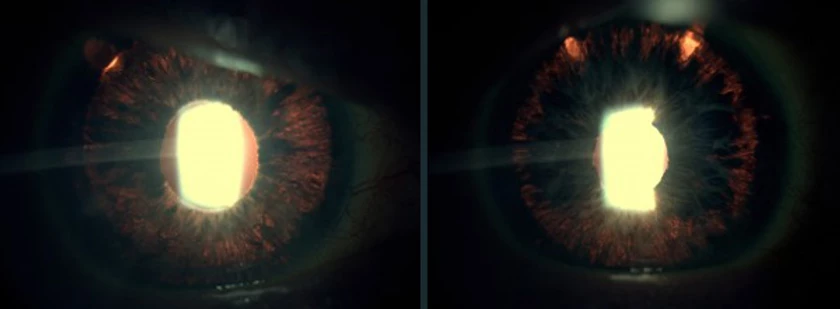
Foto derecha: en el ojo izquierdo, también es evidenciable la ganancia de pigmento, con un aumento de las áreas opacas en varias zonas de la periferia
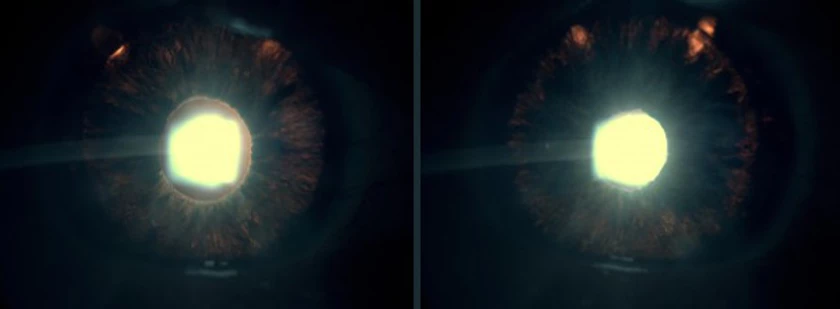
Foto derecha: igualmente, en el OI, la ganancia de pigmento es significativa, haciéndose manifiesta al comparar la imagen con la obtenida antes del tratamiento
Cirugía filtrante. Cuando la medicación y el láser fallan y necesitamos un control efectivo de la PIO, tenemos que recurrir a la cirugía. Ciertas técnicas preconizadas recientemente, como la aspiración trabecular no han demostrado ser eficaces. La EPNP o la trabeculectomía, según la experiencia y preferencias del cirujano, serán las opciones de primera elección. Si se usan antimitóticos, tener en cuenta, por la miopía y la juventud de los pacientes, la posibilidad de hipotonías. Tener en cuenta también el mayor riesgo de alteraciones regmatógenas y desprendimiento de retina en estos pacientes, por lo que la estabilidad y la compartimentalización de las diferentes cámaras es un objetivo a preservar.
